EMBL-EBI Press Office
Wellcome Genome Campus Hinxton, Cambridgeshire CB10 1SD, UK
media@ebi.ac.uk+44 1223 494369
Researchers evaluate how the new coronavirus rewires human proteins for its own replication, and identify several antiviral drugs ready for clinical trials.
An international team of researchers has analysed how SARS-CoV-2, the virus that causes COVID-19, hijacks the proteins in its target cells. The research, published in the journal Cell, shows how the virus shifts the cell’s activity to promote its own replication and to infect nearby cells. The scientists also identified seven clinically approved drugs that could disrupt these mechanisms, and recommend that these drugs are immediately tested in clinical trials.
The collaboration included researchers at EMBL’s European Bioinformatics Institute (EMBL-EBI), the Quantitative Biosciences Institute’s Coronavirus Research Group in the School of Pharmacy at University of California San Francisco (UCSF), the Howard Hughes Medical Institute, the Institut Pasteur, and the Excellence Cluster CIBSS of the University of Freiburg.
Viruses are unable to replicate and spread on their own: they need an organism – their host – to carry, replicate, and transmit them to further hosts. To facilitate this process, viruses need to take control of their host cell’s machinery and manipulate it to produce new viral particles. Sometimes, this hijacking interferes with the activity of the host’s enzymes and other proteins.
Once a protein is produced, enzymes can change its activity by making chemical modifications to its structure. For example, phosphorylation – the addition of a phosphoryl group to a protein by a type of enzyme called a kinase – plays a pivotal role in the regulation of many cell processes, including cell-to-cell communication, cell growth, and cell death. By altering phosphorylation patterns in the host’s proteins, a virus can potentially promote its own transmission to other cells and, eventually, other hosts.
The scientists used mass spectrometry, a tool to analyse the properties of a sample by measuring the mass of its molecules and molecular fragments, to evaluate all host and viral proteins that showed changes in phosphorylation after SARS-CoV-2 infection. They found that 12% of the host proteins that interact with the virus were modified. The researchers also identified the kinases that are most likely to regulate these modifications. Kinases are potential targets for drugs to stop the activity of the virus and treat COVID-19.
“The virus prevents human cells from dividing, maintaining them at a particular point in the cell cycle. This provides the virus with a relatively stable and adequate environment to keep replicating,” explains Pedro Beltrao, Group Leader at EMBL-EBI.
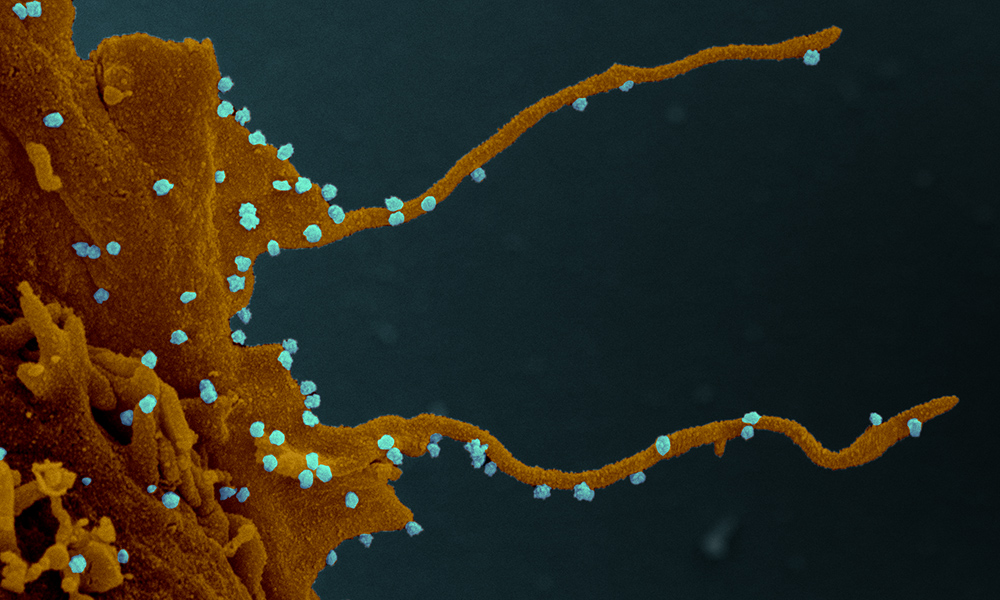
SARS-CoV-2 not only impacts cell division, but also cell shape. One of the key findings from the study is that infected cells exhibit long, branched, arm-like extensions, or filopodia. These structures may help the virus reach nearby cells in the body and advance the infection, but further study is warranted.
“The distinct visualisation of the extensive branching of the filopodia once again elucidates how understanding the biology of virus–host interaction can illuminate possible points of intervention in the disease,” says Nevan Krogan, Director of the Quantitative Biosciences Institute at UCSF and Senior Investigator at Gladstone Institutes.
“Kinases possess certain structural features that make them good drug targets. Drugs have already been developed to target some of the kinases we identified, so we urge clinical researchers to test the antiviral effects of these drugs in their trials,” says Beltrao.
In some patients, COVID-19 causes an overreaction of the immune system, leading to inflammation. An ideal treatment would relieve these exaggerated inflammatory symptoms while stopping the replication of the virus. Existing drugs targeting the activity of kinases may be the solution to both problems.
The researchers identified dozens of drugs approved by the Food and Drug Administration (FDA) or ongoing clinical trials that target the kinases of interest. Seven of these compounds, primarily anticancer and inflammatory disease compounds, demonstrated potent antiviral activity in laboratory experiments.
“Our data-driven approach for drug discovery has identified a new set of drugs that have great potential to fight COVID-19, either by themselves or in combination with other drugs, and we are excited to see if they will help end this pandemic,” says Krogan.
“We expect to build upon this work by testing many other kinase inhibitors while identifying both the underlying pathways and additional potential therapeutics that may intervene in COVID-19 effectively,” says Kevan Shokat, Professor in the Department of Cellular and Molecular Pharmacology at UCSF.
This work was funded by grants from the National Institute of Mental Health and the National Institute of Allergy and Infectious Diseases, both part of the National Institutes of Health; the Defense Advanced Research Projects Agency; the Center for Research for Influenza Pathogenesis; the Centers of Excellence for Influenza Research and Surveillance of the National Institute of Allergy and Infectious Diseases; the Centers of Excellence for Integrative Biology of Emerging Infectious Diseases of the Agence Nationale de la Recherche (France); F. Hoffmann-LaRoche AG; Vir Biotechnology, Centre for Integrative Biological Signalling Studies (CIBSS), European Research Council (ERC) and the Ron Conway Family. Shokat is a Howard Hughes Medical Institute investigator. A complete list of authors and full funding information is available in the Cell paper.
Research in the Beltrao Group
Silencing the SARS-CoV-2 receptor with epigenetic modifications
Understanding how SARS-CoV-2 behaves in the gut
Investigating the structure and mechanisms of coronavirus biomolecules
Quantitative Bioscience Institute Coronavirus Research Group

Ein internationales Forscherteam hat analysiert wie SARS-CoV-2, das Virus das COVID-19 verursacht, Proteine in seinen Wirtszellen kapert. Die Studie, im Journal Cell veröffentlicht, zeigt, wie das Virus die Funktionen der Zelle verändert, um seine eigene Vermehrung zu fördern und angrenzende Zellen zu infizieren. Die Wissenschaftler haben auch sieben Medikamente identifiziert – einige bereits zugelassen – die diese Mechanismen unterbrechen könnten und empfehlen, dass diese Medikamente sofort in klinischen Studien getestet werden.
Das Projekt war eine Zusammenarbeit bestehend aus Forschern von EMBLs Europäischem Institut für Bioinformatik (EMBL-EBI), der Coronavirus-Forschungsgruppe des Instituts für Quantitative Biowissenschaften an der School of Pharmacy der University of California San Francisco (UCSF), dem Howard Hughes Medical Institute, dem Institut Pasteur und dem Exzellenzcluster CIBSS der Universität Freiburg.
Viren können sich nicht alleine vermehren und verbreiten. Sie brauchen einen Organismus – ihren Wirt – der sie trägt, vermehrt und an neue Wirte weitergibt. Um diesen Vorgang zu ermöglichen, müssen Viren die Kontrolle über die Maschinerie ihrer Wirtszellen übernehmen und diese manipulieren, um neue Virenpartikel zu produzieren. Manchmal stört diese Übernahme die Aktivität der Enzyme und anderer Proteine der Wirtszelle.
Wenn ein Protein produziert wurde, können Enzyme seine Aktivität verändern, indem sie chemische Veränderungen an seiner Struktur vornehmen. So spielt beispielsweise Phosphorylierung – das Anfügen einer Phosphorylgruppe zu einem Protein durch eine Art von Enzym namens Kinase – eine wichtige Rolle in der Regulierung von vielen Vorgängen in der Zelle. Dazu gehört die Kommunikation zwischen Zellen, Zellwachstum und Zelltod. Indem er Phosphorylierungsmuster in den Proteinen der Wirtszelle verändert, kann das Virus möglicherweise seine Übertragung auf andere Zellen und schließlich auch auf andere Wirte fördern.
Die Wissenschaftler verwendeten Massenspektrometrie – eine Technologie, die die Eigenschaften einer Probe analysiert, indem sie die Masse ihrer Moleküle und Molekülfragmente misst – um alle Wirts- und Virenproteine zu untersuchen, die nach einer SARS-CoV-2 Infektion Veränderungen in ihrer Phosphorylierung zeigten. Sie stellten fest, dass 12% der Wirtsproteine, die mit dem Virus interagieren, verändert waren. Die Forscher identifizierten auch die Kinasen, die diese Modifizierungen am wahrscheinlichsten regulieren. Kinasen sind potenzielle Ziele für Medikamente, um die Aktivität des Virus zu stoppen und COVID-19 zu behandeln.
“Das Virus verhindert die Teilung menschlicher Zellen und hält sie an einem bestimmten Punkt im Zellzyklus fest. Dadurch erhält das Virus eine relativ stabile und angemessene Umgebung, um sich weiter zu vermehren,” erklärt Pedro Beltrao, Gruppenleiter am EMBL-EBI.
SARS-CoV-2 beeinflusst nicht nur die Zellteilung, sondern auch die Zellform. Eines der wichtigsten Ergebnisse der Studie ist, dass infizierte Zellen Filopodien aufweisen: lange, verzweigte, armähnliche Verlängerungen. Diese Strukturen könnten dem Virus dabei helfen, nahe Zellen zu erreichen und sich weiter zu verbreiten – dies bedarf jedoch weiterer Studien.
“Die ausgeprägte Visualisierung der ausgedehnten Verzweigung von Filopodien verdeutlicht einmal mehr, wie das Verständnis der Biologie hinter Virus–Wirt Interaktionen mögliche Eingriffspunkte gegen die Krankheit aufzeigen kann”, sagt Nevan Krogan, Direktor des Instituts für Quantitative Biowissenschaften an der UCSF und Senior Investigator an den Gladstone Institutes.
“Kinasen besitzen bestimmte strukturelle Merkmale die sie zu guten Zielen für Medikamente machen. Es wurden bereits Medikamente entwickelt, die gegen manche der von uns gefundenen Kinasen gerichtet sind. Deswegen appellieren wir an klinische Forscher, die antiviralen Effekte dieser Medikamente in ihren Studien zu testen”, sagt Beltrao.
In manchen Patienten verursacht COVID-19 eine Überreaktion des Immunsystems, was zu einer Entzündung führt. Eine ideale Therapie würde diese Entzündungssymptome lindern, während sie gleichzeitig die Vermehrung des Virus stoppt. Bereits existierende Medikamente, die die Aktivität der Kinasen unterbrechen, könnten eine Lösung für beide Probleme sein.
Die Forscher haben Dutzende Medikamente bestimmt, die von der Food and Drug Administration (FDA) zugelassen sind, sowie laufende klinische Studien, welche die in Frage kommenden Kinasen zum Ziel haben. Sieben dieser Verbindungen – in erster Linie krebs- und entzündungshemmende Medikamente – zeigten in Laborexperimenten starke antivirale Eigenschaften.
“Unser datenbasierter Ansatz zur Entdeckung von Medikamenten hat einen neuen Satz Medikamente bestimmt, die ein großes Potential zur Bekämpfung von COVID-19 haben – entweder alleine oder in Kombination mit anderen Mitteln. Wir sind gespannt zu sehen, ob sie dabei helfen werden diese Pandemie zu beenden”, sagt Krogan.
“Wir wollen auf dieser Arbeit aufbauen, indem wir viele weitere Kinasehemmer testen und dabei sowohl die zugrunde liegenden Mechanismen als auch zusätzliche potenzielle Therapieansätze identifizieren, die wirksam in COVID-19 eingreifen könnten ”, sagt Kevan Shokat, Professor in der Abteilung für Zelluläre und Molekulare Pharmakologie an der UCSF.
This work was funded by grants from the National Institute of Mental Health and the National Institute of Allergy and Infectious Diseases, both part of the National Institutes of Health; the Defense Advanced Research Projects Agency; the Center for Research for Influenza Pathogenesis; the Centers of Excellence for Influenza Research and Surveillance of the National Institute of Allergy and Infectious Diseases; the Centers of Excellence for Integrative Biology of Emerging Infectious Diseases of the Agence Nationale de la Recherche (France); F. Hoffmann-LaRoche AG; Vir Biotechnology, Centre for Integrative Biological Signalling Studies (CIBSS), European Research Council (ERC) and the Ron Conway Family. Shokat is a Howard Hughes Medical Institute investigator. A complete list of authors and full funding information is available in the Cell paper.
Forschung der Beltrao Gruppe
Silencing the SARS-CoV-2 receptor with epigenetic modifications
Understanding how SARS-CoV-2 behaves in the gut
Investigating the structure and mechanisms of coronavirus biomolecules
Quantitative Bioscience Institute Coronavirus Research Group

Une équipe internationale de chercheurs a analysé la façon dont le SARS-CoV-2, virus responsable du Covid-19, modifie les protéines de ses cellules hôtes. L’étude publiée dans la revue Cell montre comment le virus détourne l’activité des cellules pour assurer sa propre réplication et infecter les cellules voisines. Les scientifiques ont également identifié sept médicaments qui pourraient entraver ces mécanismes, et ils préconisent que ces médicaments soient immédiatement testés dans des essais cliniques.
Cette collaboration comprend des scientifiques de l’Institut Européen de Bioinformatique du Laboratoire Européen de Biologie Moléculaire (EMBL-EBI), du groupe de recherche sur le coronavirus de l’Institut de Biosciences Quantitatives de l’Université de Californie à San Francisco (UCSF), de l’Institut Médical Howard Hughes, de l’Institut Pasteur, et de l’Université de Freiburg.
Les virus sont incapables de se répliquer et de se propager seuls : ils ont besoin d’un organisme – leur hôte – pour les transporter, les répliquer et les transmettre à d’autres hôtes. Pour encourager ce processus, les virus doivent prendre le contrôle de la machinerie cellulaire de leur hôte et la manipuler pour qu’elle produise de nouvelles particules virales. Il arrive que ce détournement interfère avec l’activité des enzymes et autre protéines de l’hôte.
Après qu’une protéine est produite, des enzymes peuvent affecter son activité en apportant des modifications chimiques à sa structure. Par exemple, la phosphorylation – l’addition d’un groupe phosphoryl à la protéine par un type d’enzymes appelées kinases – joue un rôle majeur pour la régulation de nombreux processus cellulaires, y compris la croissance et la mort d’une cellule ainsi que sa communication avec les cellules voisines. En altérant la phosphorylation des protéines de son hôte, un virus peut potentiellement assurer sa propre transmission à d’autres cellules, voire d’autres hôtes.
Les scientifiques ont utilisé la spectrométrie de masse, un outil permettant d’analyser les propriétés d’un échantillon en mesurant la masse de ses molécules et fragments moléculaires, pour déterminer quelles protéines virales et quelles protéines de l’hôte subissent un changement de phosphorylation après une infection de SARS-CoV-2. Ils ont trouvé que 12% des protéines de l’hôte qui interagissent avec le virus étaient modifiées. Les chercheurs ont également identifié les kinases les plus susceptibles de réguler ces modifications. Les kinases sont des cibles médicamenteuses potentielles pour arrêter l’activité du virus, et pour traiter le Covid-19.
“Le virus empêche les cellules humaines de se diviser, et les maintient dans un état intermédiaire du cycle cellulaire. Ceci procure un environnement stable au virus, idéal pour sa réplication”, explique Pedro Beltrao, chef de groupe à l’EMBL-EBI.
Le SARS-CoV-2 a un impact sur la division cellulaire, mais aussi sur la forme des cellules infectées. L’une des découvertes clés de cette étude est que les cellules infectées portent de longs filopodes, des extensions filamenteuses et ramifiées. Ces structures pourraient aider le virus à atteindre des cellules avoisinantes dans le corps humain et faire progresser l’infection, cependant des recherches supplémentaires seront nécessaire pour valider cette hypothèse.
“L’embranchement considérable des filopodes démontre encore une fois comment la compréhension de la biologie des interactions virus-hôte peut mettre en lumière de potentiels points faibles de la maladie”, dit Nevan Krogan, Directeur de l’Institut de Biosciences Quantitatives à l’UCSF et Chercheur Senior aux Instituts Gladstone.
“Les kinases possèdent certaines caractéristiques structurales qui font d’elles de bonnes cibles médicamenteuses. Certains médicaments ont déjà été développés pour cibler certaines des kinases que nous avons identifiées. Nous encourageons donc d’autres chercheurs à tester les effets antiviraux de ces médicaments dans des essais cliniques”, dit Beltrao.
Chez certains patients, le Covid-19 provoque une réaction excessive du système immunitaire menant à une inflammation. Un traitement optimal soulagerait ces symptômes inflammatoires tout en bloquant la réplication du virus. Des médicaments existants ciblant l’activité de certaines kinases pourraient permettre de résoudre ces deux problèmes.
Les scientifiques ont identifié des dizaines de médicaments qui ciblent les kinases d’intérêt et sont approuvés par l’agence américaine des produits alimentaires et médicamenteux (Food and Drug Administration, FDA) ou en cours d’essais cliniques. Sept de ces composés, principalement anti-cancer ou anti-inflammatoires, démontrent des propriétés antivirales en laboratoire.
“Notre approche pour la découverte de médicaments a identifié un nouvel assortiment de médicaments qui offrent un grand potentiel pour combattre le Covid-19, soit individuellement ou en combinaison avec d’autres médicaments, et nous sommes impatients de voir s’ils vont contribuer à mettre fin à la pandémie”, dit Krogan.“Nous espérons consolider nos découvertes en testant de nombreux autres inhibiteurs de kinases, tout en identifiant les mécanismes moléculaires de ces interactions et d’autres approches thérapeutiques qui pourraient combattre efficacement le Covid-19”, dit Kevan Shokat, Professeur au département de pharmacologie cellulaire et moléculaire de l’UCSF.
This work was funded by grants from the National Institute of Mental Health and the National Institute of Allergy and Infectious Diseases, both part of the National Institutes of Health; the Defense Advanced Research Projects Agency; the Center for Research for Influenza Pathogenesis; the Centers of Excellence for Influenza Research and Surveillance of the National Institute of Allergy and Infectious Diseases; the Centers of Excellence for Integrative Biology of Emerging Infectious Diseases of the Agence Nationale de la Recherche (France); F. Hoffmann-LaRoche AG; Vir Biotechnology, Centre for Integrative Biological Signalling Studies (CIBSS), European Research Council (ERC) and the Ron Conway Family. Shokat is a Howard Hughes Medical Institute investigator. A complete list of authors and full funding information is available in the Cell paper.
La recherche du groupe de Pedro Beltrao
Silencing the SARS-CoV-2 receptor with epigenetic modifications
Understanding how SARS-CoV-2 behaves in the gut
Investigating the structure and mechanisms of coronavirus biomolecules
Quantitative Bioscience Institute Coronavirus Research Group

Un team internazionale di ricercatori ha analizzato come SARS-CoV-2, il virus che causa COVID-19, dirotta il funzionamento delle proteine nelle sue cellule bersaglio. La ricerca, pubblicata sulla rivista Cell, mostra come il virus modifica il funzionamento cellulare per potersi replicare ed infettare le cellule vicine. Gli scienziati hanno inoltre identificato sette farmaci, approvati per uso clinico, che potrebbero intercettare questi meccanismi, e ne raccomandano l’immediato utilizzo per test clinici.
La collaborazione ha coinvolto i ricercatori dell’Istituto Europeo di Bioinformatica dell’EMBL (EMBL-EBI), il gruppo di ricerca Quantitative Biosciences Institute’s Coronavirus Research Group della School of pharmacy dell’Università di California a San Francisco (UCSF), l’Howard Hughes Medical Institute, l’Institut Pasteur e l’Università di Friburgo.
I virus non sono in grado di replicarsi e diffondersi da soli: hanno bisogno di un organismo – il loro ospite – che li trasporti, consenta loro di replicarsi e di trasmettersi ad altri ospiti. Per facilitare questo processo, i virus devono controllare il funzionamento della cellula ospite e manipolarlo per produrre nuove particelle virali. A volte, questo “dirottamento” interferisce con l’attività degli enzimi dell’ospite e di altre proteine.
Quando una proteina viene prodotta, gli enzimi possono modificare la sua attività apportando modifiche chimiche alla sua struttura. Per esempio, la fosforilazione – l’aggiunta di un gruppo fosforilico a una proteina da parte di un tipo di enzima chiamato chinasi – gioca un ruolo fondamentale nella regolazione di molti processi cellulari, tra cui la comunicazione da cellula a cellula, la crescita e la morte cellulare. Alterando lo stato di fosforilazione delle proteine dell’ospite, un virus può potenzialmente promuovere la propria trasmissione ad altre cellule ed eventualmente ad altri ospiti.
Gli scienziati hanno utilizzato la spettrometria di massa, una tecnica che analizza le proprietà di un campione misurando la massa delle sue molecole e dei suoi frammenti molecolari, per analizzare tutte le proteine dell’ospite e quelle virali che mostrano cambiamenti nella fosforilazione dopo l’infezione da SARS-CoV-2. L’analisi ha rivelato che il 12% delle proteine dell’ospite che interagiscono con il virus vengono modificate. I ricercatori hanno anche identificato le chinasi che più probabilmente regolano queste modifiche. Le chinasi sono potenziali bersagli farmacologici per fermare l’attività del virus.
“Il virus impedisce alle cellule umane di dividersi arrestandole in un punto preciso del ciclo cellulare. Questo fornisce al virus un ambiente relativamente stabile e adeguato per continuare a replicarsi”, spiega Pedro Beltrao, Group Leader di EMBL-EBI.
SARS-CoV-2 non solo ha un impatto sulla divisione cellulare, ma anche sulla forma delle cellule. Uno dei risultati chiave dello studio è che le cellule infette presentano estensioni lunghe, ramificate, simili a braccia o filopodi. Queste strutture possono aiutare il virus a raggiungere le cellule vicine nel corpo e a far progredire l’infezione, ma su questo aspetto saranno necessari ulteriori studi.
“La visualizzazione dell’estesa ramificazione dei filopodi, ancora una volta, chiarisce come la comprensione della biologia dell’interazione virus-ospite possa fare luce su potenziali strategie terapeutiche nei confronti della malattia”, dice Nevan Krogan, direttore del Quantitative Biosciences Institute presso l’UCSF e Ricercatore Senior presso i Gladstone Institutes.
“Le chinasi possiedono alcune caratteristiche strutturali che le rendono bersagli farmacologici ideali. Sono già stati sviluppati alcuni farmaci per colpire alcune delle chinasi che abbiamo identificato, quindi invitiamo i ricercatori clinici a testare gli effetti antivirali di questi farmaci nei loro studi”, dice Beltrao.
In alcuni pazienti, COVID-19 provoca una reazione eccessiva del sistema immunitario, che porta all’infiammazione. Un trattamento ottimale dovrebbe quindi alleviare questi sintomi infiammatori eccessivi, arrestando la replicazione virale. I farmaci esistenti che interferiscono con l’attività delle chinasi coinvolte potrebbero dunque essere la soluzione ad entrambi i problemi.
I ricercatori hanno identificato decine di farmaci, già approvati dalla Food and Drug Administration (FDA) o in corso di valutazione clinica, che prendono di mira le chinasi di interesse. Sette di questi composti, principalmente antitumorali e infiammatori, hanno mostrato una potente attività antivirale nei test di laboratorio.
“Il nostro approccio mirato alla scoperta di nuovi farmaci sulla base dei dati disponibili ad oggi, ha identificato una nuova serie di farmaci che hanno un grande potenziale per combattere il COVID-19, da soli o in combinazione con altri farmaci, e non vediamo l’ora di sapere se saranno d’aiuto” dichiara Krogan.
“Contiamo di proseguire in questa direzione testando molti altri inibitori delle chinasi, identificando al tempo stesso sia i meccanismi del loro funzionamento che le potenziali terapie aggiuntive che possono intervenire efficacemente nel trattamento del COVID-19”, dice Kevan Shokat, professore del Dipartimento di Farmacologia Cellulare e Molecolare dell’UCSF.
This work was funded by grants from the National Institute of Mental Health and the National Institute of Allergy and Infectious Diseases, both part of the National Institutes of Health; the Defense Advanced Research Projects Agency; the Center for Research for Influenza Pathogenesis; the Centers of Excellence for Influenza Research and Surveillance of the National Institute of Allergy and Infectious Diseases; the Centers of Excellence for Integrative Biology of Emerging Infectious Diseases of the Agence Nationale de la Recherche (France); F. Hoffmann-LaRoche AG; Vir Biotechnology, Centre for Integrative Biological Signalling Studies (CIBSS), European Research Council (ERC) and the Ron Conway Family. Shokat is a Howard Hughes Medical Institute investigator. A complete list of authors and full funding information is available in the Cell paper.
Research in the Beltrao Group
Silencing the SARS-CoV-2 receptor with epigenetic modifications
Understanding how SARS-CoV-2 behaves in the gut
Investigating the structure and mechanisms of coronavirus biomolecules
Quantitative Bioscience Institute Coronavirus Research Group

Un equipo de científicos internacionales ha analizado cómo el SARS-CoV-2, el virus que causa la enfermedad COVID-19, se apodera de las proteínas en las células objetivo. La investigación, publicada en la revista científica Cell, muestra cómo el virus modifica la actividad celular para promover su réplica y así infectar células cercanas. Los investigadores también han identificado siete medicamentos ya aprobados que podrían perturbar dichos mecanismos, y recomiendan que se inicien los análisis clínicos con esos medicamentos de inmediato.
La colaboración ha contado con investigadores del Instituto de Bioinformática Europeo (EMBL-EBI), el grupo de investigación en Coronavirus del Instituto de Biociencias Cuantitativas de la Universidad de California San Francisco (USCF), del Howard Hughes Medical Institute, del Instituto Pasteur y de la Universidad de Friburgo.
Los virus no son capaces de reproducirse y propagarse independientemente: necesitan un organismo – el portador o huésped – para transportarse, replicarse y transmitirse a siguientes portadores. Para facilitar este proceso, los virus necesitan tomar el control del mecanismo celular de los portadores y manipularlo para producir nuevas partículas virales. A veces, esta toma de control interfiere en las enzimas y proteínas del huésped.
Cuando se produce una proteína, las enzimas pueden cambiar su actividad haciendo modificaciones químicas en su estructura. Por ejemplo, la fosforilación – la adición de un grupo fosfato a una proteína a través de una enzima llamada quinasa – juega un papel fundamental en la regulación de varios procesos celulares, incluyendo la comunicación entre células, el crecimiento celular y la muerte celular. Si se altera la fosforilación en los patrones de las proteínas del portador, el virus puede, potencialmente, promover su propia transmisión a otras células y, con el tiempo, a otros portadores.
Los investigadores han usado la espectrometría de masas, una herramienta para analizar las propiedades de una muestra midiendo la masa de sus moléculas y de los fragmentos moleculares, para evaluar todas las proteínas del huésped y del virus que han mostrado cambios en la fosforilación después de una infección de SARS-CoV-2. Los científicos han visto que el 12% de las proteínas del portador que interactuaron con el virus habían sido modificadas. Además, los investigadores también han identificado las quinasas más propensas a regular esas modificaciones. Las quinasas son objetivos potenciales de los medicamentos para detener la actividad del virus y poder tratar la COVID-19.
“El virus impide la división de células humanas y las mantiene en un punto concreto del ciclo celular. Esto proporciona al virus un entorno relativamente estable y adecuado para continuar replicándose”, explica Pedro Beltrao, Investigador Principal del EMBL-EBI.
El SARS-CoV-2 no sólo afecta a la división celular, sino que también influye en la forma celular. Uno de los descubrimientos clave de este estudio es que las células infectadas muestran largas extensiones ramificadas, o filopodios. Estas estructuras podrían ayudar al virus a alcanzar células cercanas y expandir la infección, aunque se necesitaría un estudio más a fondo de esta cuestión.
“Esta visualización tan específica de las extensiones ramificadas de los filopodios dilucida la comprensión biológica entre la interacción virus-portador y ayuda a identificar posibles puntos de intervención en la enfermedad”, dice Nevan Krogan, Director del Instituto de Biociencias Cuantitativas de la UCSF e Investigador Senior del Gladstone Institutes.
“Las quinasas poseen ciertas características estructurales que las hacen buenos objetivos para medicamentos. Algunos medicamentos ya fueron desarrollados para atacar algunas de las quinasas que hemos identificado. Por ese motivo instamos a los investigadores clínicos a que prueben los efectos antivirales de esos medicamentos en sus ensayos”, dice Beltrao.
En algunos pacientes, la COVID-19 causa una reacción excesiva del sistema inmune, que conduce a inflamación. Un tratamiento ideal debería aliviar estos síntomas inflamatorios al mismo tiempo que detiene la reproducción del virus. Los fármacos existentes que interfieren con la actividad de las quinasas podrían ser la solución a ambos problemas.
Los investigadores han encontrado docenas de fármacos aprobados por la Food and Drug Administration (FDA) o ensayos clínicos en curso que tienen cómo objetivo las quinasas de interés. Siete de esos compuestos, principalmente compuestos anticancerígenos y antiinflamatorios, han demostrado una actividad antiviral potente en experimentos de laboratorio.
“Nuestro enfoque basado en datos para el descubrimiento de fármacos ha identificado siete nuevos fármacos que tienen gran potencial para luchar contra la COVID-19, ya sea individualmente o en combinación con otros medicamentos, y estamos entusiasmados por saber si podrán ser de ayuda para acabar con esta pandemia”, dice Krogan.
“Esperamos poder continuar trabajando en este estudio, probando otros inhibidores de quinasas al tiempo que identificamos su funcionamiento y otras terapias potenciales que podrían intervenir en la COVID-19 de manera eficaz”, dice Kevan Shokat, Profesor del Departamento de Farmacología Celular y Molecular de la UCSF.
This work was funded by grants from the National Institute of Mental Health and the National Institute of Allergy and Infectious Diseases, both part of the National Institutes of Health; the Defense Advanced Research Projects Agency; the Center for Research for Influenza Pathogenesis; the Centers of Excellence for Influenza Research and Surveillance of the National Institute of Allergy and Infectious Diseases; the Centers of Excellence for Integrative Biology of Emerging Infectious Diseases of the Agence Nationale de la Recherche (France); F. Hoffmann-LaRoche AG; Vir Biotechnology, Centre for Integrative Biological Signalling Studies (CIBSS), European Research Council (ERC) and the Ron Conway Family. Shokat is a Howard Hughes Medical Institute investigator. A complete list of authors and full funding information is available in the Cell paper.
Research in the Beltrao Group
Silencing the SARS-CoV-2 receptor with epigenetic modifications
Understanding how SARS-CoV-2 behaves in the gut
Investigating the structure and mechanisms of coronavirus biomolecules
Quantitative Bioscience Institute Coronavirus Research Group