Focus on: Insulin
Descrizione
Questa risorsa didattica vi guiderá attraverso vari passggi consecutivi ad esplorare la struttura biologica della molecola dell’insulina – dalla struttura primaria alla quaternaria.
Come iniziare:
- Selezionate il livello di struttura proteica su cui volete lavorare usando la tabulazione.
- Raccogliete informazioni sui dettagli strutturali dell’insulina ed eseguite gli esercizi.
- Cercate di rispondere alle domande dell’ Insulin quiz.
- La Scheda Insulina puó essere stampata e usata per mettere alla prova le vostre conoscenze sulla biologia strutturale dell’insulina. Colorate le strutture ed esploratele in 3D!
Info
L’insulina viene inizialmente sintetizzata come preproinsulina, un polipeptide formato da 110 aminoacidi che contiene sequenze addizionali:
- Una sequenza “pre” amino-terminale (peptide segnale di 24 aminoacidi), che permette la secrezione della proteina.
- Una sequenza “pro” centrale (il peptide C di 35 aminoacidi) che determina il folding corretto della proteina.
Dopo che la preproinsulina é stata tradotta nel reticolo endoplasmatico, un enzima taglia i 24 aminoacidi amino-terminali, producendo la proinsulina che si piega e permette la formazione dei ponti disolfuro fra i residui di cisteina.
A questo stadio, la proteina passa nell’apparato del Golgi, dove il peptide C viene rimosso e si forma l’insulina matura, che si accumula nelle vescicole di Golgi.
L’ insulina matura é formata da due catene polipeptidiche (catena A e catena B). La catena A é costituita da 21 aminoacidi, la catena B da 30.
Prim.
L’insulina matura è costituita da due catene polipeptidiche (catene A e B). la catena A è costituita da 21 aminoacidi, la catena B da 30 aminoacidi (le sequenze sono riportate sotto).
Compito
Confrontate le catene A (e le catene B) dell’insulina umana e suina allineando le sequenze aminoacidiche. Ci sono differenze nella sequenza degli aminoacidi?
- Copiate le due sequenze dell’insulina umana e suina che trovate sotto. Selezionate e copiate tutto il blocco di sequenze a partire da >sp per la catena A (step 1) e poi per la catena B (step 2).
- Incollate le sequenze nel campo di ricerca di MUSCLE (tasti Ctrl. + V).
- Nella sezione “STEP 2″ assicuratevi che“Output Format” sia su“ClustalW”.
- Cliccate sul tasto “Submit” e il software eseguirà il vostro allineamento.
- Dopo qualche secondo appariranno i risultati. Date un’occhiata all’allineamento e rispondete alle domande del quiz.
Nota: Per inviare il secondo set di sequenze è necessario ricaricare la pagina per avere il campo di ricerca MUSCLE vuoto.
Step 1 – Confrontate le catene A:
>sp|P01308|90-110, Insulina, catena A, Umana
GIVEQCCTSICSLYQLENYCN
>sp|P01315|88-108, Insulina, catena A, maiale
GIVEQCCTSICSLYQLENYCN
Step2 – Confrontate le catene B:
>sp|P01308|25-54, Insulina, catena B, Umana
FVNQHLCGSHLVEALYLVCGERGFFYTPKT
>sp|P01315|25-54,Insulina, catena B, maiale
FVNQHLCGSHLVEALYLVCGERGFFYTPKA
Sec.
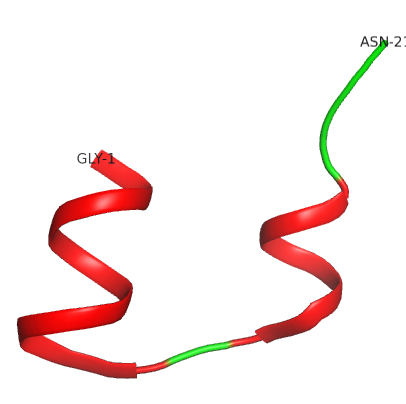
La struttura secondaria è determinata da due alfa-eliche nella catena A.
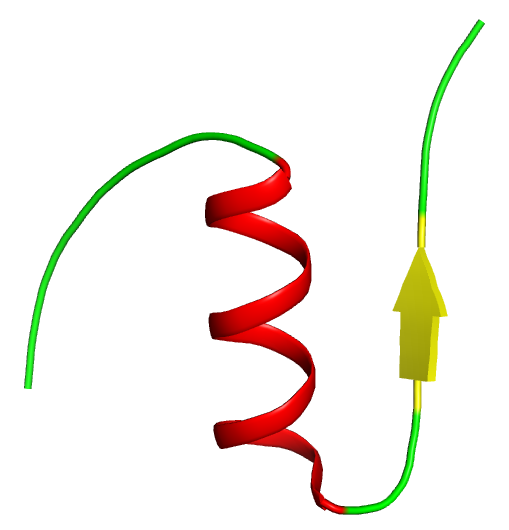
La catena B ha una sezione al alfa-elica e una regione a foglietto-beta. Si ripiega attorno alla catena A (vedi struttura terziaria).
Terz.
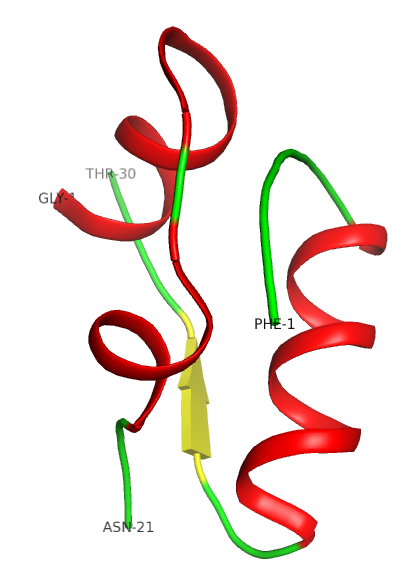
La struttura terziaria è stabilizzata da ponti disolfuro (vedi insulina – scheda). La parte esterna della proteina è polare, quella interna é sostanzialmente idrofobica.
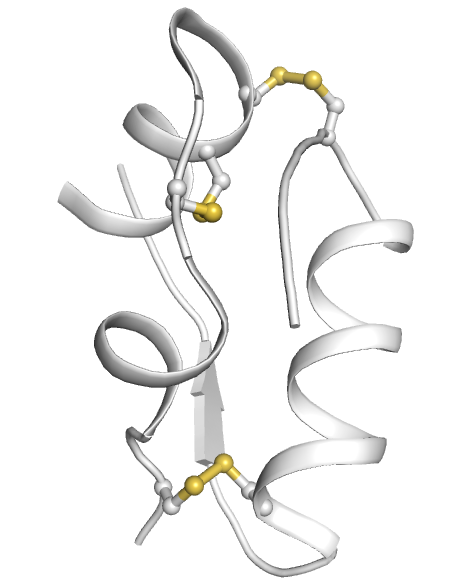
L’insulina é formata da due catene polipeptidiche (A e B) tenute insieme da due ponti disolfuro; un terzo ponte disolfuro é situato all’interno della catena A.
Quat.
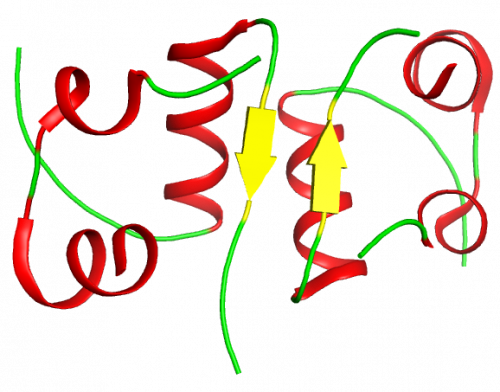
Per quanto riguarda la struttura quaternaria l’insulina tende a formaredimeri in soluzione, dovuti alla formazione di legami a idrogeno tra le estremità C-terminali della catena B.
Scheda
Pima di tutto scaricate il documento Insulina – scheda e stampatelo.
Compiti
- Usate i vostri occhiali stereo per esplorare la struttura della proteina in 3D (in alto a sinistra).
- Colorate la catena A secondo lo schema dei colori.
- Colorate la catena B secondo lo schema dei colori.
- Colorate le seguenti strutture sulla struttura disegnata a destra:
- alfa-eliche
- folglietti beta
- ponti disolfuro
Schema dei colori:
- alfa eliche– rosso
- foglietti beta – giallo
- parti della proteina prive di struttura – verde
- Ponti disolfuro – arancio
- Parte N-terminale della proteina – blu
- Parte C-terminale della proteina – rosa
Quiz
Prova l’ Insulin Quize verifica la tua conoscenza di questa sorprendente molecola.
Extra material
Guardate la EMBL Insight Lecture 2013 “From Code to Function – Observing Protein Synthesis Through the Electron Microscope”
Christiane Schaffitzel and her team study the function and three-dimensional structure of ribosomes using a combination of molecular biology, biochemistry and cryo-electron microscopy. In her talk, Christiane gives an overview of the steps involved in protein synthesis and the role ribosomes play in the process. She then illustrates how her research group uses cryo-electron microscopy to study the structures of these fascinating molecules. Christiane’s central research questions are: what we can learn from the make up of these fascinating molecules and how are synthesised proteins targeted to their destinations?
Topic area: Structural & Computational biology
Age group: 16-19
Share:
 English
English Deutsch
Deutsch Français
Français